Produktname:Calciumcarbid
Molekulares Format:C2Ca
CAS-Nr.:75-20-7
Molekularstruktur des Produkts:
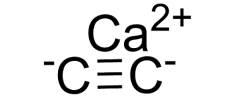
Calciumcarbid (Molekülformel: CaC2) ist ein wichtiger chemischer Rohstoff, der bei der chemischen Verarbeitung von Kalkstein entsteht. Im Jahr 1892 entwickelten H. Maysan (Franzose) und H. Wilson (USA) gleichzeitig ein Verfahren zur Herstellung von Calciumcarbid, das auf Ofenreduktion basierte. Die USA erreichten 1895 erfolgreich die industrielle Produktion. Die Eigenschaften von Calciumcarbid hängen von seiner Reinheit ab. Das Industrieprodukt ist meist eine Mischung aus Calciumcarbid und Calciumoxid und enthält auch Spuren von Schwefel, Phosphor, Stickstoff und anderen Verunreinigungen. Mit zunehmendem Gehalt an Verunreinigungen verfärbt es sich grau, braun bis schwarz. Schmelzpunkt und elektrische Leitfähigkeit nehmen mit abnehmender Reinheit ab. Die Reinheit des Industrieprodukts beträgt normalerweise 80 % und der Schmelzpunkt liegt zwischen 1.800 und 2.000 °C. Bei Zimmertemperatur reagiert es nicht mit Luft, kann aber bei über 350 °C oxidieren und bei 600 bis 700 °C mit Stickstoff zu Calciumcyanamid reagieren. Calciumcarbid erzeugt bei Kontakt mit Wasser oder Dampf Acetylen und setzt dabei große Mengen Wärme frei. CaC2 + 2H2O─ → C2H2 + Ca (OH) 2 + 125185,32 J, 1 kg reines Calciumcarbid kann 366 l Acetylen (366 l) (15 °C, 0,1 MPa) produzieren. Daher ist Calciumcarbid bei der Lagerung streng von Wasser fernzuhalten. Es wird üblicherweise in einem versiegelten Eisenbehälter verpackt und manchmal in einem trockenen Lagerhaus gelagert, das bei Bedarf mit Stickstoff gefüllt wird.
Calciumcarbid (CaC2) hat einen knoblauchartigen Geruch und reagiert mit Wasser zu Acetylengas, Calciumhydroxid und Wärme. Früher wurde es in Grubenlampen verwendet, um kontinuierlich eine kleine Acetylenflamme zu erzeugen und so in Kohlebergwerken für etwas Beleuchtung zu sorgen.
Calciumcarbid wird als Entschwefelungsmittel, Stahlentwässerungsmittel, Brennstoff in der Stahlherstellung, starkes Desoxidationsmittel und als Acetylengasquelle verwendet. Es dient als Ausgangsstoff für die Herstellung von Calciumcyanamid, Ethylen, Chloroprenkautschuk, Essigsäure, Dicyandiamid und Cyanidacetat. Es wird in Karbidlampen und Spielzeugkanonen wie der Urknallkanone und der Bambuskanone verwendet. Es wird mit Calciumphosphid in schwimmenden, selbstentzündlichen Schiffssignalen verwendet. Calciumcarbid ist aufgrund seiner wichtigen Rolle als Grundlage der Acetylenindustrie das industriell wichtigste Karbid. An Orten mit Erdölknappheit Calciumcarbiddient als Ausgangsstoff für die Herstellung von Acetylen (1 kg Carbid ergibt ca. 300 Liter Acetylen), das wiederum als Baustein für eine Reihe organischer Chemikalien (z. B. Vinylacetat, Acetaldehyd und Essigsäure) dient. An einigen Standorten wird Acetylen auch zur Herstellung von Vinylchlorid verwendet, dem Rohstoff für die PVC-Produktion.
Eine weniger wichtige Verwendung von Calciumcarbid ist in der Düngemittelindustrie bekannt. Es reagiert mit Stickstoff zu Calciumcyanamid, dem Ausgangsstoff für die Herstellung von Cyanamid (CH2N2). Cyanamid ist ein gängiges landwirtschaftliches Produkt zur Förderung der frühen Blattbildung.
Calciumcarbid kann auch als Entschwefelungsmittel zur Herstellung von schwefelarmem Kohlenstoffstahl eingesetzt werden. Es wird auch als Reduktionsmittel zur Herstellung von Metallen aus ihren Salzen verwendet, z. B. zur direkten Reduktion von Kupfersulfid zu metallischem Kupfer. Darüber hinaus ist es an der Reduktion von Kupfersulfid zu metallischem Kupfer beteiligt.
Chemwin kann Industriekunden eine breite Palette an Kohlenwasserstoffen und chemischen Lösungsmitteln in großen Mengen anbieten.Bitte lesen Sie vorher die folgenden grundlegenden Informationen zur Geschäftsbeziehung mit uns:
1. Sicherheit
Sicherheit hat für uns oberste Priorität. Neben der Aufklärung unserer Kunden über die sichere und umweltschonende Nutzung unserer Produkte ist es uns ein Anliegen, die Sicherheitsrisiken für Mitarbeiter und Auftragnehmer auf ein sinnvolles und praktikables Minimum zu reduzieren. Daher fordern wir den Kunden auf, vor unserer Lieferung sicherzustellen, dass die entsprechenden Sicherheitsstandards für Entladung und Lagerung eingehalten werden (siehe HSSE-Anhang in den Allgemeinen Geschäftsbedingungen). Unsere HSSE-Experten beraten Sie gerne zu diesen Standards.
2. Lieferart
Kunden können Produkte bei chemwin bestellen und liefern lassen oder direkt aus unserem Produktionswerk beziehen. Als Transportmittel stehen LKW, Bahn und multimodaler Transport zur Verfügung (es gelten gesonderte Bedingungen).
Bei Kundenanforderungen können wir die Anforderungen von Binnenschiffen oder Tankern spezifizieren und spezielle Sicherheits-/Überprüfungsstandards und -anforderungen anwenden.
3. Mindestbestellmenge
Wenn Sie Produkte über unsere Website kaufen, beträgt die Mindestbestellmenge 30 Tonnen.
4.Zahlung
Die Standardzahlungsmethode ist die Zahlung per Lastschrift innerhalb von 30 Tagen nach Rechnungsstellung.
5. Lieferdokumente
Folgende Dokumente liegen jeder Lieferung bei:
· Frachtbrief, CMR-Frachtbrief oder anderes relevantes Transportdokument
· Analyse- oder Konformitätszertifikat (falls erforderlich)
· HSSE-bezogene Dokumentation gemäß den Vorschriften
· Zollrechtliche Dokumentation (falls erforderlich)
Produktkategorien
-

Telefon
-

E-Mail
-

Whatsapp
-

Spitze


















